Neuer Mechanismus der krankhaften Gefäßneubildung im diabetischen Auge entdeckt
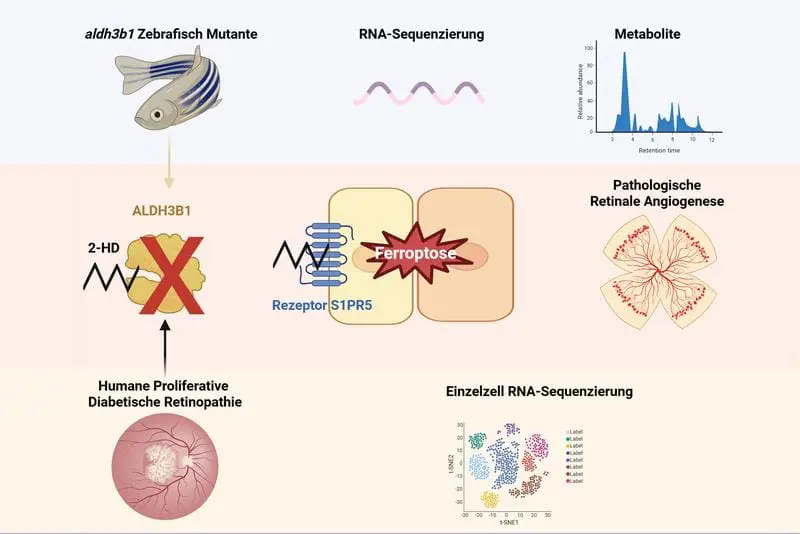
Ein internationales Forschungsteam unter Leitung von Professor Dr. Jens Kroll von der Medizinischen Fakultät Mannheim der Universität Heidelberg hat einen bisher unbekannten molekularen Mechanismus der pathologischen Gefäßneubildung im Auge aufgeklärt. Der Prozess spielt eine zentrale Rolle bei schweren Augenerkrankungen wie der diabetischen Retinopathie und der altersbedingten Makuladegeneration, die zu bleibenden Sehstörungen bis hin zur Erblindung führen können.
Im Mittelpunkt steht der Botenstoff Sphingosin-1-Phosphat (S1P) und sein Abbauprodukt 2-Hexadecenal (2-HD). Die Forscher konnten zeigen, dass ein Überschuss von 2-HD den S1P-Rezeptor 5 (S1PR5) hemmt. Dies führt zu einer Störung des Eisenhaushalts in den Zellen, löst Ferroptose (einen eisenabhängigen, durch Lipidperoxidation getriebenen Zelltod) aus und fördert dadurch die krankhafte Neubildung von Blutgefäßen in der Netzhaut.
Die Ergebnisse wurden in der Fachzeitschrift Nature Communications veröffentlicht. Die Studien nutzten unter anderem das Zebrafisch-Modell sowie Daten von Patienten. Durch gezielte Blockade von 2-HD oder Stabilisierung des S1PR5-Rezeptors konnte die pathologische Gefäßbildung im Tiermodell deutlich reduziert werden.

Vielversprechender Therapieansatz
Besonders relevant ist, dass bereits zugelassene Medikamente existieren, die den S1PR5-Rezeptor modulieren (derzeit vor allem bei Multipler Sklerose eingesetzt). Diese könnten potenziell auch für die Behandlung von Augenerkrankungen genutzt werden und eine Alternative oder Ergänzung zu den derzeitigen VEGF-Hemmern darstellen, die häufig wiederholt gespritzt werden müssen und Nebenwirkungen haben können.
„Die neu identifizierte Signalachse rund um 2-Hexadecenal und S1PR5 eröffnet alternative medikamentöse Therapieansätze, die gezielter und möglicherweise nebenwirkungsärmer wirken könnten“, so Professor Kroll.
Die Studie liefert neue Einblicke in die Pathogenese von diabetischen Augenerkrankungen und könnte langfristig zu wirksameren und patientenfreundlicheren Behandlungen führen. Weitere Untersuchungen sollen nun klären, wie sich dieser Mechanismus therapeutisch nutzen lässt.
Original Paper:
Lesen Sie auch:
Erhöhte Glukagonspiegel bei Typ-2-Diabetes bereits früh nach Diagnose nachweisbar – MedLabPortal
Redaktion: X-Press Journalistenbüro GbR
Gender-Hinweis. Die in diesem Text verwendeten Personenbezeichnungen beziehen sich immer gleichermaßen auf weibliche, männliche und diverse Personen. Auf eine Doppel/Dreifachnennung und gegenderte Bezeichnungen wird zugunsten einer besseren Lesbarkeit verzichtet.