SPOT sagt passende Transporter-Substrat-Paare voraus
Für den ständigen Austausch von Stoffen in und aus einer biologischen Zelle heraus sind Transportproteine verantwortlich. Es ist aber schwierig zu bestimmen, welche Stoffe ein bestimmtes Protein transportieren kann. Bioinformatiker der Heinrich-Heine-Universität Düsseldorf (HHU) haben nun mithilfe Künstlicher Intelligenz (KI) ein SPOT genanntes Modell entwickelt, das dies mit hoher Genauigkeit vorhersagen kann.
Ständig müssen Stoffe in biologische Zellen durch die Zellmembran hinein- oder heraustransportiert werden, damit diese überleben und ihre Funktion erfüllen können. Aber längst nicht alle Stoffe, die sich durch den Körper bewegen, sollen in die Zelle gelangen. Und manche dieser Transportvorgänge müssen steuerbar sein, etwa nur zu bestimmter Zeit oder unter bestimmten Bedingungen funktionieren, um eine Zellfunktion auszulösen.
Die Rolle dieser aktiven und spezialisierten Transportkanäle übernehmen sogenannte Transportproteine oder kurz Transporter, von denen viele unterschiedliche in die Zellmembranen eingebaut sind. Ein Transportprotein besteht aus einer großen Zahl einzelner Aminosäuren, die insgesamt eine komplexe dreidimensionale Struktur bilden.
Jeder Transporter ist auf ein ganz bestimmtes Molekül – das sogenannte Substrat – oder eine kleine Gruppe von Substraten spezialisiert. Doch auf welche genau? Forschende suchen immer wieder nach den passenden Paaren von Transportern und Substraten.
Prof. Martin Lercher von der Arbeitsgruppe für Computational Cell Biology und Korrespondenzautor einer nun in PLOS Biology erschienenen Studie: „Experimentell zu bestimmen, welche Substrate zu welchen Transportern passen, ist schwierig. Schon die dreidimensionale Struktur eines Transporters – aus der man gegebenenfalls auf die Substrate schließen kann – zu ermitteln ist eine Herausforderung, denn sobald man die Proteine aus der Membran herauslöst, werden sie instabil.“
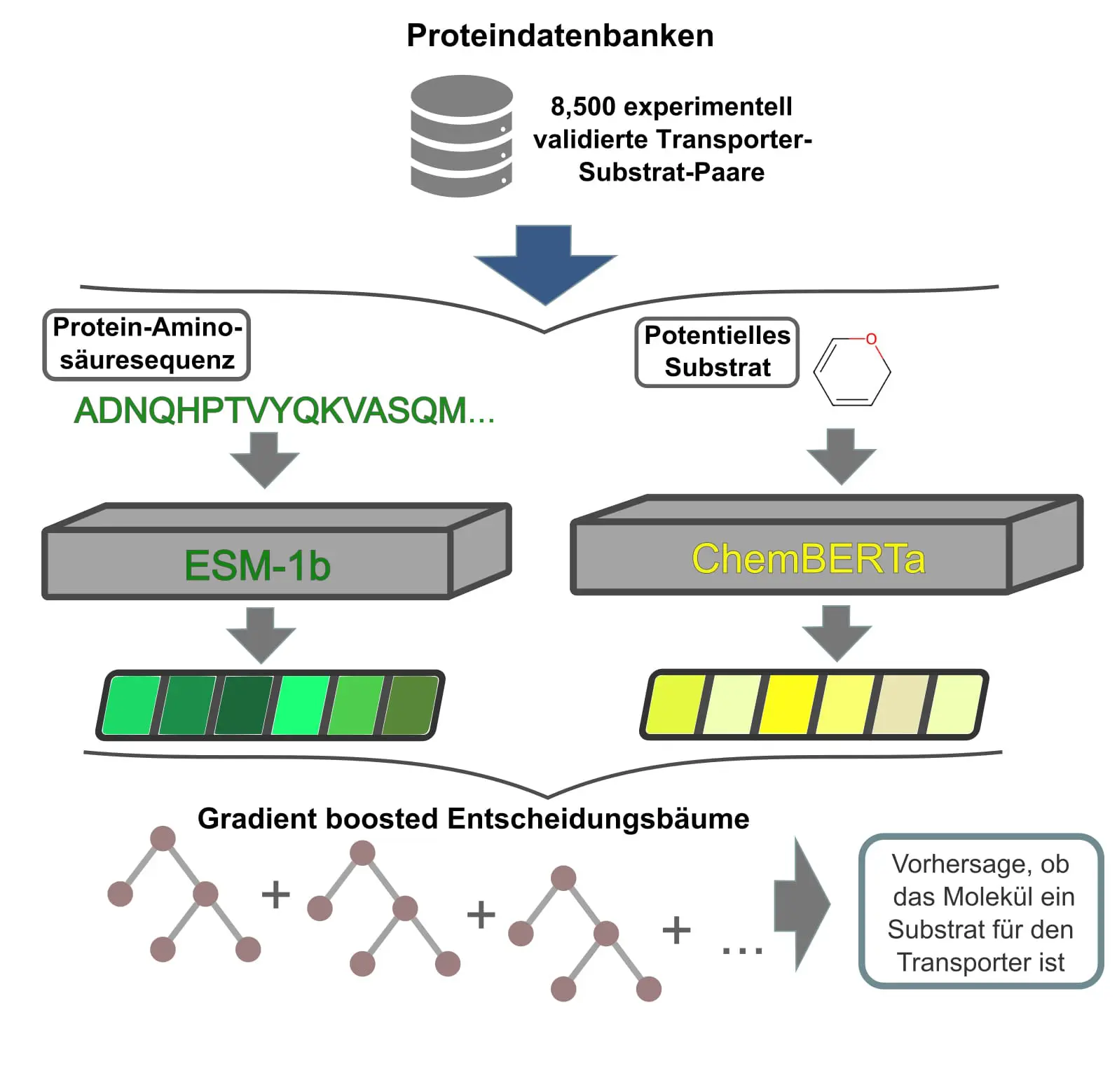
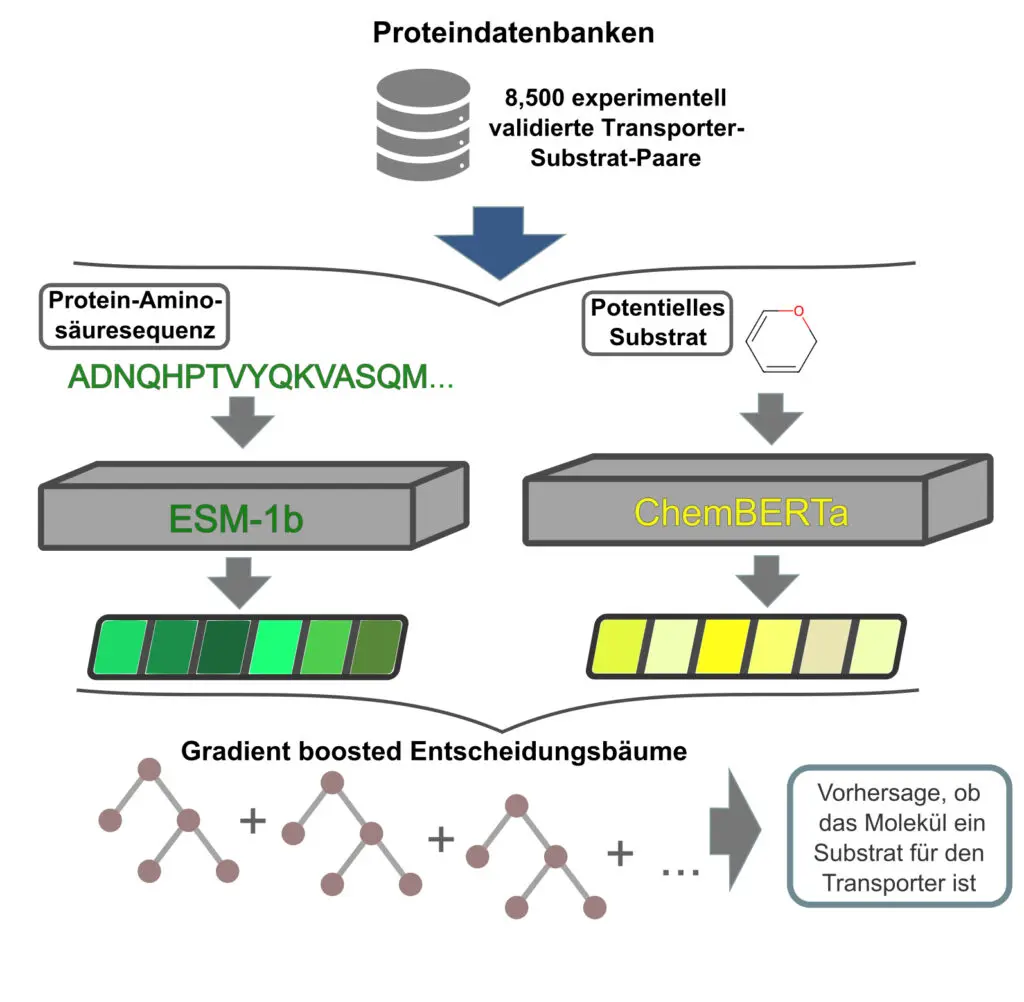
„Wir haben einen anderen, einen KI-basierten Ansatz gewählt“, sagt Dr. Alexander Kroll, Erstautor der Studie. „Unsere SPOT genannte Methode nutzte für ein Deep Learning-Modell über 8.500 bereits experimentell validierte Transporter-Substrat-Paare als Trainingsdatensatz.“
Damit ein Computer die Transporterproteine und Substratmoleküle verarbeiten kann, verwandeln die Düsseldorfer Bioinformatiker die Proteinsequenzen und Substratmoleküle zunächst jeweils in numerische Vektoren, die von KI-Modellen verarbeitet werden können. Nach dem fertigen Lernprozess kann dann der Vektor für einen neuen Transporter und diejenige für möglicherweise passende Substrate in das KI-System eingegeben werden. Das Modell gibt eine Vorhersage, mit einer wie hohen Wahrscheinlichkeit bestimmte Substrate zu dem Transporter passen.
Die Forschenden haben das fertig angelernte Modell mit einem unabhängigen Testdatensatz überprüft, dessen Transporter-Substrat-Paarungen ebenfalls bekannt waren. Mit einer Genauigkeit von über 92 Prozent sagte SPOT voraus, ob irgendein Molekül ein Substrat für einen speziellen Transporter ist.
SPOT schlägt also vielversprechende Substratkandidaten vor. „Wir können so den Suchraum für Experimentatoren sehr stark einschränken. Sie können dann viel schneller im Labor tatsächlich herausfinden, welches Substrat sicher zu einem Transporter passt“, erläutert Prof. Lercher das Zusammenspiel von bioinformatischer Vorhersage und experimenteller Verifizierung. Dies gelte für jedes beliebige Transportprotein, nicht nur – wie bei bisherigen Ansätzen – für eingeschränkte Klassen ähnlicher Proteine.
Das Modell hat verschiedene denkbare Anwendungsfelder. so könnten beispielsweise in der Biotechnologie Stoffwechselwege so verändert werden, dass bestimmte Produkte, etwa Biokraftstoffe, hergestellt werden. Oder aber es könnten Arzneimittel auf Transporter hin angepasst werden, so dass diese leichter in genau die Zelle gelangen, wo sie wirken sollen.
Originalpublikation
Lesen Sie auch
Jetzt Online: Atlas der Proteine soll Demenz und Krebs bekämpfen helfen – MedLabPortal
Bioinformatik: Internet-Toolkit aus Deutschland revolutioniert Proteindesign – MedLabPortal
Die Beiträge im News-Bereich werden erstellt vom X-Press Journalistenbüro
Gender-Hinweis. Die in diesem Text verwendeten Personenbezeichnungen beziehen sich immer gleichermaßen auf weibliche, männliche und diverse Personen. Auf eine Doppel/Dreifachnennung und gegenderte Bezeichnungen wird zugunsten einer besseren Lesbarkeit verzichtet.