Chronische Oxycodon-Exposition in der Schwangerschaft beeinträchtigt fetale Herzentwicklung
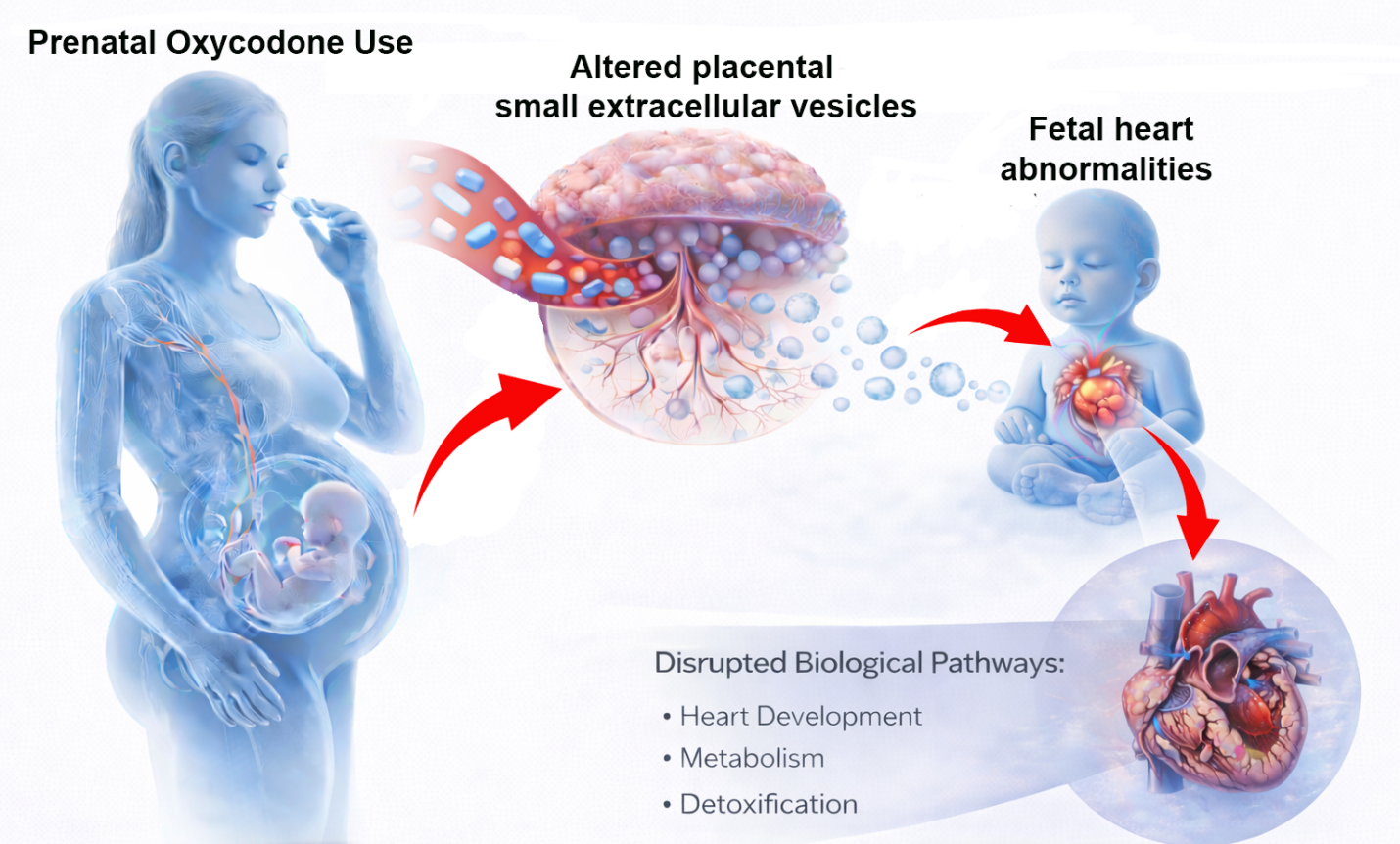
Die chronische Oxycodon-Exposition während der Schwangerschaft führt zu tiefgreifenden Veränderungen im Proteom plazentarer kleiner extrazellulärer Vesikel (PSEVs) und beeinträchtigt molekulare Signalwege, die mit fetaler Kardiomyopathie in Verbindung stehen. Das zeigt eine neue präklinische Studie des University of Nebraska Medical Center, die in der Fachzeitschrift Extracellular Vesicles and Circulating Nucleic Acids veröffentlicht wurde.
Die Wissenschaftler um Gurudutt Pendyala und Sowmya V. Yelamanchili untersuchten in einem etablierten Rattenmodell die Auswirkungen einer chronischen mütterlichen Oxycodon-Behandlung auf die Zusammensetzung und Funktion plazentarer EVs. Diese Vesikel dienen als wichtige Botenstoffträger zwischen Mutter und Fetus und spielen eine zentrale Rolle bei der fetalen Organentwicklung.
Von 456 identifizierten EV-Proteinen waren 107 signifikant dysreguliert. Besonders auffällig war die deutliche Herunterregulation von Proteinen wie Atp2a2 (Calcium-Handhabung im Herzmuskel), Lmna (Kernstabilität), Tgfb3 (Gewebe-Remodellierung), Agt (Blutdruckregulation) und Sgce (Membranstabilität im Herzmuskel). Diese Veränderungen betreffen zentrale Signalwege der hypertrophen und dilatativen Kardiomyopathie. Zusätzlich zeigten sich Störungen im Energiestoffwechsel (TCA-Zyklus, Fettsäureabbau), in der Glykosylierung und im vesikulären Transport.
Die EVs aus oxycodon-exponierten Plazenten waren zudem kleiner und in höherer Konzentration vorhanden, was auf veränderte Biogenese oder Stress-induzierte Vesikulation hinweist.
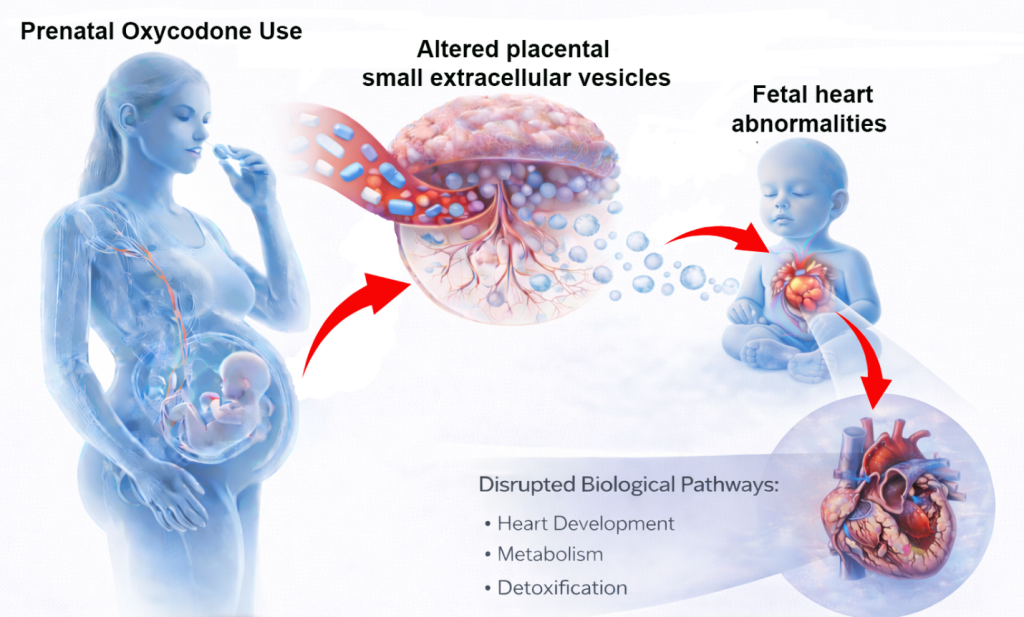
Opioide wie Oxycodon werden in den USA auch in der Schwangerschaft häufig zur Schmerztherapie eingesetzt, führen jedoch zu einer wachsenden Zahl von Neugeborenen mit Entzugssymptomen und langfristigen Entwicklungsrisiken. Die Plazenta fungiert nicht nur als Nährstoff- und Sauerstoffversorger, sondern auch als aktiver Signalgeber über EVs. Störungen in diesem System können die fetale Herz- und Gefäßentwicklung nachhaltig beeinträchtigen.
Die Studie liefert erstmals eine detaillierte proteomische Charakterisierung plazentarer EVs nach chronischer Oxycodon-Exposition und verbindet diese mit bekannten Kardiomyopathie-Pfaden. Die Ergebnisse sind methodisch solide (Kombination aus TEM, NTA, Western Blot und label-free Proteomik) und werden durch bioinformatische Analysen gut untermauert. Die Übereinstimmung mit humanen MASH-Daten in einer früheren Studie der gleichen Arbeitsgruppe unterstreicht die Relevanz des Modells.
Es handelt sich allerdings um ein präklinisches Rattenmodell. Daher müssen Unterschiede in Plazentastruktur, Pharmakokinetik und fetaler Entwicklung zwischen Ratte und Mensch berücksichtigt werden. Die Stichprobengröße ist moderat, und eine unabhängige Validierung einzelner Proteine (z. B. per Western Blot oder targeted Assays) steht noch aus. Langzeitstudien zur tatsächlichen Herzfunktion der Nachkommen fehlen bisher.
Dennoch bietet die Arbeit einen wichtigen mechanistischen Einblick und unterstreicht das Potenzial plazentarer EVs als Biomarker für opioid-bedingte Entwicklungsrisiken. Sie legt den Grundstein für weitere translationale Forschung und mögliche EV-basierte Diagnostik oder Interventionen in der Perinatalmedizin.
Original Paper:
Redaktion: X-Press Journalistenbüro GbR
Gender-Hinweis. Die in diesem Text verwendeten Personenbezeichnungen beziehen sich immer gleichermaßen auf weibliche, männliche und diverse Personen. Auf eine Doppel/Dreifachnennung und gegenderte Bezeichnungen wird zugunsten einer besseren Lesbarkeit verzichtet.