Universität Basel entwickelt Enzym für nachhaltige MHAT-Reaktion
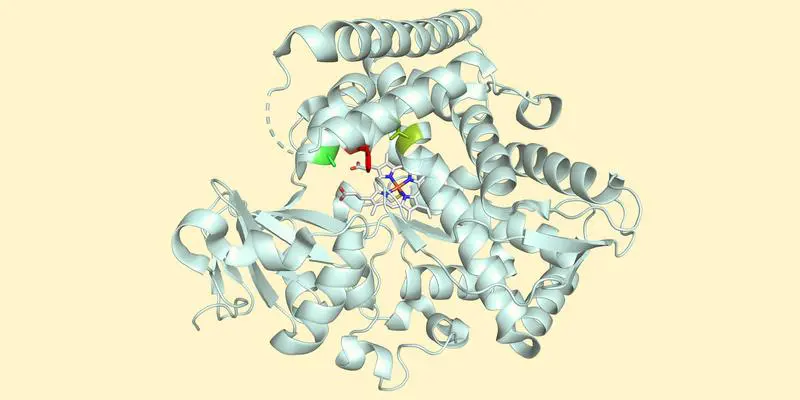
Forschende der Universität Basel haben ein natürliches Enzym so modifiziert, dass es die anspruchsvolle Metallhydrid-Wasserstoffatom-Transfer-Reaktion (MHAT) katalysiert. Diese Innovation ermöglicht eine umweltfreundlichere und effizientere Herstellung komplexer Moleküle für Arzneistoffe und Feinchemikalien, wie in der Fachzeitschrift «Nature» veröffentlicht wurde.
Katalysatoren sind zentrale Werkzeuge der grünen Chemie, da sie chemische Reaktionen beschleunigen, Energie sparen und Abfall reduzieren. Die MHAT-Reaktion gilt als vielversprechende Methode, um aus zweidimensionalen Substraten komplexe, dreidimensionale Moleküle mit spezifischen Funktionen zu erzeugen. Dabei überträgt ein Metallhydrid ein Wasserstoffatom auf einen Kohlenwasserstoff, wodurch eine reaktive Stelle entsteht, die mit einer funktionellen Gruppe verknüpft wird. Die Herausforderung besteht darin, die präzise dreidimensionale Anordnung der Atome zu kontrollieren, da spiegelbildliche Moleküle – sogenannte Enantiomere – unterschiedliche biologische Wirkungen haben können, was in der Pharmaindustrie entscheidend ist.

Unter der Leitung von Prof. Dr. Thomas R. Ward nutzte das Forschungsteam das Schlüssel-Schloss-Prinzip natürlicher Enzyme. Sie modifizierten ein Hämoprotein, sodass die MHAT-Reaktion in dessen aktivem Zentrum abläuft. Durch die spezifische Struktur dieser Enzym-Tasche wird in 98 von 100 Fällen das gewünschte Enantiomer produziert, da das Spiegelbild nicht hineinpasst. Diese Präzision ist mit herkömmlichen chemischen Methoden schwer zu erreichen. Zudem arbeitet das Enzym energieeffizient und umweltfreundlich, was es für nachhaltige Anwendungen attraktiv macht.
Die Forschung, Teil des Nationalen Forschungsschwerpunkts «Molecular Systems Engineering», ebnet den Weg für umweltfreundlichere Produktionsprozesse in der Pharma- und Feinchemie. Eine Herausforderung bleibt die Anpassung des Enzyms an andere Ausgangsstoffe, da dessen Spezifität sowohl Vorteil als auch Einschränkung ist. Die Forschenden arbeiten nun an Lösungen für dieses Problem sowie an nachhaltigeren Wegen zur Herstellung des Metallhydrids.
Original Paper:
Repurposing haemoproteins for asymmetric metal-catalysed H atom transfer | Nature
Die Beiträge im News-Bereich werden erstellt vom X-Press Journalistenbüro
Gender-Hinweis. Die in diesem Text verwendeten Personenbezeichnungen beziehen sich immer gleichermaßen auf weibliche, männliche und diverse Personen. Auf eine Doppel/Dreifachnennung und gegenderte Bezeichnungen wird zugunsten einer besseren Lesbarkeit verzichtet.