Neudefinition der Analytik kleiner Moleküle: Überbrückung der Lücke zwischen LC–MS/MS und Immunoassays
Kleine Moleküle (Small Molecule Compounds, SMCs) sind essenzielle Biomarker in der klinischen Diagnostik und Therapieüberwachung. Ihre präzise, hochdurchsatzfähige und zugleich kosteneffiziente Bestimmung stellt jedoch nach wie vor eine zentrale Herausforderung in der Laboratoriumsmedizin dar.
SMCs (Molekulargewicht <1000 Da), einschließlich Schilddrüsenhormone, Sexualhormone, Vitamine und partiell auch Arzneistoffe, sind von zentraler Bedeutung für die klinische Diagnostik und das Therapiemonitoring [1]. Aufgrund ihrer geringen Größe, einfachen Struktur und eines einzelnen Erkennungsepitops sind klassische Sandwich-Immunoassays nicht anwendbar [2]. Daher basiert die Routinediagnostik überwiegend auf kompetitiven Immunoassays. Diese bestimmen die Analytkonzentration über Konkurrenzmechanismen, sind jedoch anfällig für Matrixeffekte, was häufig zu eingeschränkter Sensitivität, reduzierter Genauigkeit im Niedrigkonzentrationsbereich und einem begrenzten Messbereich führt.
Derzeit dominieren LC–MS/MS und kompetitive Immunoassays die SMC-Analytik. LC–MS/MS bietet eine hohe Spezifität und ermöglicht Spurenanalysen, erfordert jedoch aufwendige Geräteausstattung, spezialisiertes Personal und ist durch einen begrenzten Probendurchsatz eingeschränkt. Kompetitive Immunoassays hingegen sind automatisiert und breit verfügbar, weisen jedoch häufig Defizite in der analytischen Präzision auf. Die Kombination der Vorteile beider Ansätze stellt seit Langem ein zentrales Ziel dar.
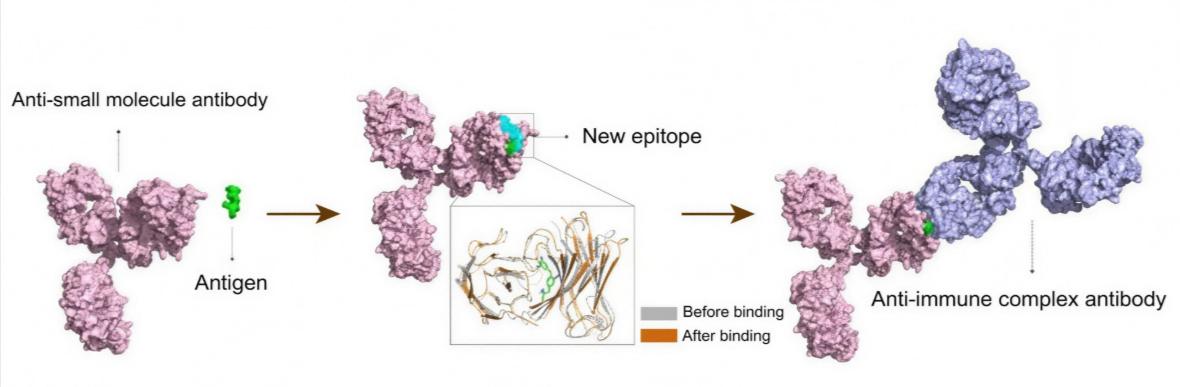
Vor diesem Hintergrund wurden nichtkompetitive Immunoassays für kleine Moleküle intensiv untersucht [2,5]. Im Gegensatz zu kompetitiven Verfahren ermöglichen sie eine direkte Detektion des Analyten und verbessern dadurch Sensitivität und Reproduzierbarkeit. Eine besonders innovative Entwicklung stellt die Noncompetitive Anti-Immune Complex Assay (NACA)-Technologie dar.

Die NACA-Technologie nutzt sekundäre Anti-Immunkomplex-Antikörper, die neu gebildete Epitope erkennen, welche durch die Bindung zwischen Primärantikörper und Zielmolekül entstehen [3,4]. Dieser Mechanismus verstärkt die Antigen-Antikörper-Interaktion, erhöht die Bindungsstabilität und maximiert die Effizienz der Analytbindung, wodurch die analytische Genauigkeit deutlich verbessert wird.
Als einer der frühen Anwender hat Snibe diese Technologie erfolgreich von der Forschung in die klinische Routine überführt und die Snibe-NACA-Plattform etabliert. Diese adressiert die zentralen Schwächen konventioneller Methoden und bietet fünf wesentliche Vorteile:
- Hohe Übereinstimmung mit LC–MS/MS
- Breiter linearer Messbereich für unterschiedliche klinische Anwendungen
- Hohe Sensitivität, insbesondere im Niedrigkonzentrationsbereich
- Hohe Spezifität mit ausgeprägter Störresistenz
- Hoher Durchsatz bei gleichzeitig hoher Kosteneffizienz
Durch diese Eigenschaften ermöglicht die Plattform eine präzise und skalierbare Analytik kleiner Moleküle bei minimalem manuellen Aufwand und schafft ein ausgewogenes Verhältnis zwischen analytischer Leistungsfähigkeit und operativer Effizienz.
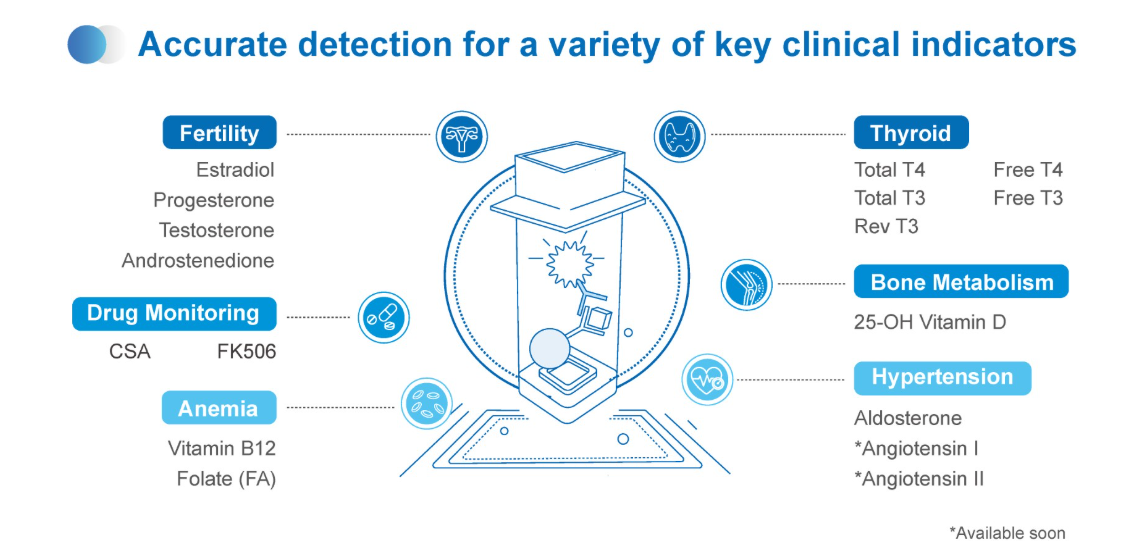
Bis heute werden NACA-basierte Systeme in über 100 Ländern eingesetzt und haben mehr als 50 Millionen Testergebnisse generiert. Die Anwendungen erstrecken sich über verschiedene Fachgebiete, darunter Endokrinologie, Onkologie und Reproduktionsmedizin, und unterstützen eine frühzeitige Diagnosestellung sowie personalisierte Therapieansätze.
Zukünftige Entwicklungen zielen darauf ab, die Sensitivität weiter zu steigern, das Testportfolio auszubauen und die Integration in digitale Gesundheitslösungen zu ermöglichen. Durch die enge Verzahnung von technologischer Innovation und klinischem Bedarf wird erwartet, dass diese Fortschritte sowohl die diagnostische Präzision erhöhen als auch neue Einblicke in biologische Prozesse liefern.
Reference:
[1] Li Y, et al. TrAC Trends in Analytical Chemistry, 2018, 103: 198-208.
[2] Self C H, et al. Clinical chemistry, 1994, 40(11): 2035-2041.
[3] Nemazee D A, et al. Proceedings of the National Academy of Sciences, 1982, 79(12): 3828-3832.
[4] Voss Jr E W, et al. Molecular Immunology, 1988, 25(8): 751-759.
[5] Pulli T, et al. Analytical Chemistry, 2005, 77(8): 2637-2642.
Weitere Informationen finden Sie auf https://www.snibe.com/en/
Für die Inhalte der Rubrik “Corporate News” sind die jeweiligen Unternehmen verantwortlich



