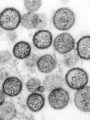
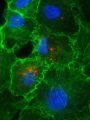
Fallbericht: Antiangiogene Therapie als Hoffnungsträger im Kampf gegen das pulmonale NUT-Mittellinienkarzinom
Das primäre pulmonale Nukleäre Protein des Testis (NUT)-Mittellinienkarzinom (NMC) ist eine äußerst seltene, hochaggressive maligne Erkrankung des Brustraums, die erhebliche diagnostische und therapeutische Herausforderungen mit sich bringt und durch heterogene klinische Manifestationen, häufige Fehldiagnosen und eine schlechte Prognose gekennzeichnet ist.
Dieser Fallbericht beschreibt zwei Patienten mit fortgeschrittenem primärem pulmonalem NMC, die mit einer multimodalen Strategie behandelt wurden, die antiangiogene Wirkstoffe, platinbasierte Chemotherapie und Strahlentherapie kombinierte – und eine Gesamtüberlebenszeit (OS) von 32 bzw. 13 Monaten erzielte, was die derzeit berichtete mediane OS von etwa 6,7 Monaten für fortgeschrittenes NMC weit übertrifft.
Es wurde auch eine systematische Literaturrecherche von 86 veröffentlichten Fällen (2011–2024) durchgeführt, in der die aktuellen Diagnosemethoden (wie die Immunhistochemie für die nukleäre NUT-Expression und die Fluoreszenz-in-situ-Hybridisierung (FISH) für die NUTM1-Umlagerung) und die Behandlungsmodalitäten für NMC zusammengefasst wurden.
Die Ergebnisse deuten laut Autoren darauf hin, dass eine multimodale Therapie mit antiangiogenen Wirkstoffen im Vergleich zur konventionellen Monotherapie zu überlegenen klinischen Ergebnissen führt, insbesondere bei Patienten, die für eine Operation nicht in Frage kommen.
Der Bericht hebt auch diagnostische Fallstricke hervor, wie z. B. überlappende histopathologische Merkmale mit Plattenepithelkarzinomen, und unterstreicht, wie die Integration einer antiangiogenen Therapie die aggressive Biologie von NMC angeht und eine neue therapeutische Richtung für diese refraktäre Malignität bietet. Der erste Patient, ein 31-jähriger Nichtraucher, stellte sich im April 2021 mit einem seit einem Monat anhaltenden Husten vor. Eine kontrastverstärkte Thorax-Abdominal-CT zeigte eine 4,7 cm × 3,4 cm große Masse an der Bronchialwurzel des rechten Mittellappens, begleitet von einer mediastinalen/hilären Lymphadenopathie und dem Verdacht auf Fernmetastasen (Lungen- und linke Magenlymphknoten), die als IVA (cT3N3M1b) eingestuft wurden. Die transbronchiale Biopsie zeigte schlecht differenzierte Epithelzellen mit fokaler Plattenepitheldifferenzierung (Keratinperlen), und die Immunhistochemie bestätigte eine diffuse nukleäre NUT-Expression sowie positive Plattenepithelmarker (CK5/6, CK7, p40) und negative neuroendokrine/thyroidale Marker.
Die Next-Generation-Sequenzierung (NGS) identifizierte eine BRD4-NUTM1-Umlagerung, was die Diagnose bestätigte. Die Erstlinientherapie umfasste sechs Zyklen Albumin-gebundenes Paclitaxel plus Cisplatin (Mai–Oktober 2021), wodurch eine partielle Remission (PR) erreicht wurde, gefolgt von einer gleichzeitigen Strahlentherapie (50 Gy/25 Fraktionen) der linken Magenlymphknoten zur lokoregionalen Kontrolle. Im Dezember 2021 wurde eine antiangiogene Therapie mit Anlotinib begonnen, wodurch die Erkrankung bis August 2022 stabil blieb (15 Monate progressionsfreies Überleben, PFS). Nachfolgende Therapielinien (BET-Inhibitor, Immuntherapie, Histon-Deacetylase-Inhibitor) konnten das Fortschreiten der Erkrankung nicht kontrollieren, und der Patient verstarb im Januar 2024 an einem multiplen Organversagen (MODS) mit einer Gesamtüberlebenszeit (OS) von 32 Monaten – das 4,8-Fache der medianen OS bei fortgeschrittenem NMC. Die zweite Patientin, eine 26-jährige Nichtraucherin, wurde zufällig bei einer Routineuntersuchung mit einer 10,0 cm × 5,5 cm großen lobulären Masse im rechten mittleren unteren Lungenlappen, hilarer/mediastinaler Lymphadenopathie und bilateralen adnexalen/pelvinen Metastasen (größte Läsion 22 cm × 13 cm) diagnostiziert, die als IVB (cT4N2M1c) eingestuft.
Biopsien der Lungen- und Beckenläsionen zeigten ein schlecht differenziertes Karzinom mit geografischer Nekrose und fokaler Keratinisierung; die Immunhistochemie bestätigte die nukleäre NUT-Expression und Plattenepithelmarker (CK5/6, p40, p63), während FISH eine NUTM1-Umlagerung nachwies. Die Erstlinientherapie (Tislelizumab, Paclitaxel-Liposom, Nedaplatin) wurde nach einem Zyklus aufgrund von starkem Gewichtsverlust, Müdigkeit und ausbleibender Läsionsreduktion abgebrochen. Die Zweitlinienbehandlung umfasste sechs Zyklen mit Paclitaxel-Albumin-Konjugat, Cisplatin und Bevacizumab (antiangiogener Wirkstoff), wobei nach zwei Zyklen eine partielle Remission (PR) und danach eine Stabilisierung der Erkrankung erreicht wurde, gefolgt von zwei Zyklen einer Erhaltungstherapie (Paclitaxel-Albumin + Bevacizumab). Nach 7 Monaten trat eine Progression (neue Hiluslymphadenopathie) auf (PFS = 7 Monate). Die hypofraktionierte Strahlentherapie (37,5 Gy/15 Fraktionen) kontrollierte die primären/mediastinalen Läsionen, jedoch nicht die Peritonealkarzinose; die anschließende Kombinationstherapie (Gemcitabin, Nedaplatin, Anlotinib, Durvalumab) wurde aufgrund einer Hepatotoxizität 3. Grades und einer Pneumonie abgebrochen. Der Patient verstarb 13 Monate nach der Diagnose an akutem hypoxischem Lungenversagen – fast doppelt so lange wie die mediane OS bei metastasiertem NMC.
Die Literaturrecherche hob kritische diagnostische Herausforderungen hervor: 22 % der Fälle wurden zunächst falsch diagnostiziert, am häufigsten als Plattenepithelkarzinom aufgrund überlappender immunhistochemischer Marker (CK5/6+, p40+, TTF-1–/Syn–). Die nukleäre NUT-Expression mittels IHC und FISH (C52-Klon, 100 % Spezifität) ist der diagnostische Goldstandard, obwohl NGS auch NUTM1-Fusionen nachweisen kann (87 % der NMC-Fälle betreffen BRD4-NUTM1) und somit eine zusätzliche Bestätigung liefert. Therapeutisch zeigten traditionelle Monotherapien oder konventionelle multimodale Therapien (Chemotherapie ± Strahlentherapie) eine begrenzte Wirksamkeit mit einer medianen PFS von 2,1 Monaten. Im Gegensatz dazu verbesserte die Integration von antiangiogenen Wirkstoffen (Anlotinib, Bevacizumab) in den beiden Fällen die Chemotherapie durch vaskuläre Normalisierung, reduzierte die Tumorhypoxie zur Verbesserung der Strahlenempfindlichkeit und hemmte die Ausbreitung durch Herunterregulierung VEGF-bezogener Signalwege (CXCR4, MMP9) – wodurch PFS und OS verlängert wurden. Während BET-Inhibitoren und Immuntherapien in präklinischen Studien vielversprechend waren, ist ihre klinische Wirksamkeit nach wie vor begrenzt, was die Notwendigkeit einer frühzeitigen Integration der antiangiogenen Therapie in die Behandlung von NMC unterstreicht.
Der Bericht stellt den therapeutischen Pessimismus in Bezug auf NMC in Frage und schlägt eine antiangiogene multimodale Therapie als praktikable Strategie zur Verbesserung der Ergebnisse bei dieser seltenen, aggressiven Malignität vor.
Original Paper:
Redaktion: X-Press Journalistenbüro GbR
Gender-Hinweis. Die in diesem Text verwendeten Personenbezeichnungen beziehen sich immer gleichermaßen auf weibliche, männliche und diverse Personen. Auf eine Doppel/Dreifachnennung und gegenderte Bezeichnungen wird zugunsten einer besseren Lesbarkeit verzichtet.