Konstanzer Forscher entschlüsseln Enzym-Mechanismus gegen Krebs
Ein internationales Forschungsteam unter Leitung von Biologen der Universität Konstanz hat einen molekularen Mechanismus entschlüsselt, der die Aktivität von N-Myristoyltransferasen reguliert. Diese Enzyme spielen in biologischen Signalwegen eine Rolle, deren Fehlregulation zur Entstehung schwerer Krankheiten wie Krebs führen kann. Die Ergebnisse der Studie, die in der Fachzeitschrift Molecular Cell veröffentlicht wurden, wurden von Wissenschaftlern der Universität Konstanz gemeinsam mit Kollegen der ETH Zürich und des California Institute of Technology erzielt.
Proteine bilden die grundlegenden Bausteine des Lebens und werden in Zellen kontinuierlich produziert, transportiert und abgebaut. Störungen in diesen Prozessen können zu schweren Erkrankungen führen. Die Forscher untersuchten die Steuerung der N-Myristoyltransferasen, Enzyme, die Proteine während ihrer Herstellung chemisch modifizieren und damit ihre Funktion ermöglichen. Diese Modifikationen betreffen Signalwege, die bei Krebs und Viruserkrankungen eine Rolle spielen. Die Studie beleuchtet den Mechanismus, durch den diese Enzyme am Ausgang der zellulären Proteinfabriken, den Ribosomen, aktiviert werden, und identifiziert einen potenziellen Ansatzpunkt für neue Medikamente.
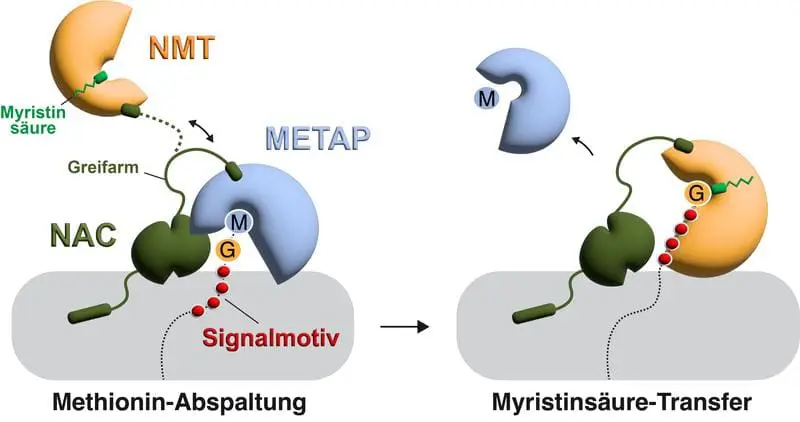
Die Proteinproduktion beginnt mit der Übersetzung genetischer Informationen in Aminosäureketten, gefolgt von chemischen Modifikationen. Häufig wird die Aminosäure Methionin abgespalten, in manchen Fällen folgt das Anhängen einer Fettsäure durch N-Myristoyltransferasen. Das Team analysierte, wie diese Enzyme am Ribosom wirken und mit konkurrierenden Enzymen interagieren.

Mithilfe struktureller, quantitativer und genetischer Methoden sowie biochemischer Experimente wurde festgestellt, dass der nascent polypeptide-associated complex eine zentrale Rolle bei der Koordinierung spielt. Dieser Komplex positioniert Enzyme am ribosomalen Tunnel, wo Proteine entstehen. Da Bindungsstellen überschneiden, erfolgt ein kontrollierter Austausch: Zuerst die Methionin-Abspaltung, dann die Fettsäure-Anhängung, ausgelöst durch ein Signalmotiv im Protein, das nach der Abspaltung freigelegt wird.
Der nascent polypeptide-associated complex reguliert auch andere Enzyme, die Acetylgruppen anhängen, eine häufigere Modifikation. Die N-Myristoyltransferasen binden dichter am Tunnel und gewinnen dadurch einen zeitlichen Vorsprung, um trotz Konkurrenz zu wirken.
Die Entschlüsselung des Mechanismus eröffnet neue Wege für Medikamente gegen Krebs und Viruserkrankungen. Bisherige Wirkstoffe hemmen die Enzyme zellweit und verursachen Nebenwirkungen. Die Studie identifiziert die Bindungsstelle zwischen Enzymen und dem nascent polypeptide-associated complex als selektiven Ansatzpunkt für gezieltere Therapien mit potenziell weniger Toxizität.
Original Paper:
Mechanism of cotranslational protein N-myristoylation in human cells: Molecular Cell
Lesen Sie auch:
Liquid Biopsy: Innovativer Test nutzt RNA zum Nachweis von Krebs im Frühstadium – MedLabPortal
Redaktion: X-Press Journalistenbüro GbR
Gender-Hinweis. Die in diesem Text verwendeten Personenbezeichnungen beziehen sich immer gleichermaßen auf weibliche, männliche und diverse Personen. Auf eine Doppel/Dreifachnennung und gegenderte Bezeichnungen wird zugunsten einer besseren Lesbarkeit verzichtet.